LAS DISOLUCIONES
RESOLUCIÓN del problema nº 17:
¿Cómo se prepararían 50 g. de una disolución de BaCl2 al 12% en peso a partir de agua pura y BaCl2.2H20 ? ¿Qué cantidad de agua y de sal necesitaríamos? (Sol.: con 7,04 g de sal y 42,96 g de agua)
Hemos de tener en cuenta que la sal de BaCl2.2H20 ya contiene algo de agua en su molécula y que cuando se disuelve, este agua de cristalización pasa a formar parte del disolvente ya que en ese momento el soluto es exclusivamente BaCl2
De esta forma, en los 50 g de disolución hay un 12% de BaCl2: 50 . 0,12 = 6 gramos
Por tanto, hemos de coger una cantidad de sal: BaCl2.2H20 en la que existan 6 g de BaCl2:
La masa molecular es: BaCl2 => 137,33 + 2.35,45 = 208,23
BaCl2.2H20 => 137,33 + 2.35,45 + 2.18 = 244,23
Y partiendo de esa relación tenemos
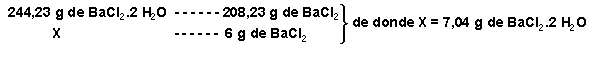
Por lo que hemos de coger 7,04 g de BaCl 2 .2H 2 O y el resto : 50 - 7,037 = 42,96 g de agua pura