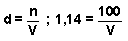 de donde V = 87,72 ml, con lo que el cuadro quedará:
de donde V = 87,72 ml, con lo que el cuadro quedará:| Soluto | Disolvente | Disolución |
| 32,00 g + | 68,00 g | = 100,00 g |
| 87,72 ml |
con lo que la molaridad es: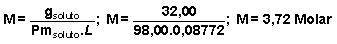
b) Por otra parte, la cantidad de soluto: Ác. Sulfúrico que tendremos en la disolución que se quiere preparar ha de salir de los 40 mL de la disolución que se tienen inicialmente:
| Soluto | Disolvente | Disolución |
| 14,59 g + | 31,01 g | = 45,60 g |
| 40 ml |
Partiendo de los 40 ml, y conociendo la densidad de la disolución inicial, calculamos la masa de la
disolución: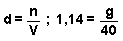 ; g = 45,60 g de disolución.
; g = 45,60 g de disolución.
y de esta cantidad, el 32% es soluto (ác. Sulfúrico); 45,60 . 0,32 = 14,59 g de soluto ác. Sulfúrico, por lo que el resto de la masa total serán de disolvente: 45,60 - 14,59 = 31,01g de agua
Con estos datos también puede calcularse la molaridad, que será:
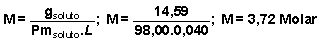 obviamente, es el mismo resultado que con los datos
anteriores ya
que se trata de la misma disolución
obviamente, es el mismo resultado que con los datos
anteriores ya
que se trata de la misma disolución
Continuando con estros datos, hemos de determinar ahora el volumen de la disolución 1 Molar (es la concentración que debe tener la disolución que nos piden) que se puede preparar con los 14,59 g de soluto ác. Sulfúrico y para ello partimos de la expresión de la Molaridad aunque ahora conocemos el valor de la Molaridad (1 Molar) y la cantidad de soluto (14,59 g de ác. Sulfúrico), por lo que de esta forma determinaremos el volumen que nos hace falta:
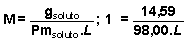 L = 0,149 litros de disolución !Molar que pueden obtenerse
L = 0,149 litros de disolución !Molar que pueden obtenerse
L = 0,149 ml , y si se disponía ya de 40 ml, el resto del volumen es el volumen de agua que se debe añadir : 149 - 40 = 109 ml de agua destilada deben añadirse
